MATERI ELEKTOKIMIA (ELKETROLISIS DAN HUKUM FARADAY BESERTA SOAL2)
MATERI KIMIA KELAS XII SEMESTER 1 SEL ELEKTROKIMIA
Elektrokimia merupakan cabang ilmu kimia yang membahas hubungan reaksi redoks dengan energi listrik. Keduanya berlangsung dalam sebuah alat yang disebut sel elektrokimia.
a. Reaksi Redoks Spontan
Reaksi redoks spontan adalah reaksi redoks yang terjadi dengan sendirinya.
Misalnya apabila logam seng dicelupkan ke dalam larutan tembaga(II)sulfat, CuSO4. Lihat gambar berikut,
Logam seng (Zn) akan larut dengan melepas elektron membentuk ion seng (Zn2+), sementara ion tembaga (Cu2+) menangkap elektron dari logam seng dan membentuk endapan tembaga (Cu). Dalam reaksi tersebut terjadi transfer elektron secara langsung dari logam Zn ke ion Cu2+. Reaksi yang terjadi,
b. Rangkaian Sel Volta
Zn + Cu2+ → Zn2++ Cu
Transfer elektron secara langsung pada reaksi di atas tidak akan menghasilkan arus listrik, oleh karena itu Luigi Galvani dan Alessandro Guiseppe Volta menemukan cara untuk menghasilkan arus listrik yaitu memisahkan logam Zn dan ion Cu2+ di wadah yang berbeda dalam suatu rangkaian yang disebut sel volta.
 |
| Rangkaian Sel volta |
Setelah rangkaian terhubung dengan baik, lempengan logam Zn teroksidasi menjadi ion Zn2+ yang akan larut di dalam larutan ZnSO4 dan melepas elektron.
Zn → Zn2++ 2e
Elektron yang dilepas akan mengalir melalui kabel listrik melewati voltmeter menuju lempengan logam Cu. Kemudian elektron tersebut akan ditangkap oleh ion Cu2+ yang berasal dari larutan CuSO4 membentuk endapan Cu.
Cu2+ + 2e → Cu
Elektron mengalir dari anoda ke katoda, sedangkan aliran arus sebaliknya mengalir dari katoda ke anoda.Faktanya tanpa jembatan garam, elektron tidak mengalir. Hal ini karena terjadinya kelebihan muatan pada kedua wadah yang berisi larutan ZnSO4 dan larutan CuSO4. Di wadah pertama yang berisi larutan ZnSO4 akan mengalami kelebihan muatan positif karena terbentuk ion Zn2+ hasil reaksi oksidasi logam Zn, sementara di wadah kedua akan mengalami kelebihan muatan negatif SO42-karena ion Cu2+ jumlahnya berkurang.
Jembatan garam berfungsi untuk menetralkan kelebihan muatan pada kedua larutan tersebut, ion Na+ akan bergerak menuju larutan CuSO4 untuk menetralkan kelebihan muatan negatif dan ion SO42- bergerak menuju larutan ZnSO4 yang kelebihan muatan positif.
Lempengan logam Zn dan Cu disebut elektroda, elektroda tempat terjadinya reaksi oksidasi disebut anoda sedangkan elektroda tempat terjadinya reaksi reduksi disebut katoda. Logam yang bertindak sebagai anoda pada sel volta di atas adalah Zn, sementara Cu bertindak sebagai katoda. Anoda dalam sel volta disebut juga elektroda negatif dan katoda sebagai elektroda positif.
c. Diagram Sel Volta
a. Deret Volta
b. Potensial Elektroda
c. Potensial Sel
2. Sel Elektrolisis
a. Kaedah Elektrolisis
b. Aspek Kuantitatif Elektrolisis
Hukum Faraday I
b. Potensial Elektroda
c. Potensial Sel
2. Sel Elektrolisis
a. Kaedah Elektrolisis
Hukum Faraday I
Massa zat yang dihasilkan pada elektrolisis berbanding lurus dengan muatan listrik yang dialirkan.Hukum Faraday II
Massa zat-zat yang dihasilkan oleh muatan listrik yang sama sebanding dengan berat ekivalen dari zat-zat tersebut.
Sel elektrokimia adalah suatu aplikasi penerapan reaksi redoks yang terdiri dari katoda (reduksi) dan anoda (oksidasi) yang menggunakan larutan elektrolit sebagai penghantar elektron. Ada dua macam sel elektrokimia yang akan kita pelajari hari ini, yaitu:
1. Sel Volta (Sel Galvani)
Sel volta adalah sel elektrokimia yang mengubah energi kimia menjadi energi listrik. Rangkaian sel volta dapat ditulis dalam bentuk notasi. Dalam menuliskan notasi sel, anoda dituliskan di sebelah kiri dan katoda di sebelah kanan yang dipisahkan oleh jembatan garam ( || ). Secara umum, notasi sel dapat dituliskan sebagai berikut:
Untuk menunjukkan kecenderungan reduksi, kita menggunakan poetensial reduksi standar atau lebih dikenal dengan sebutan potensial elektroda standar. Untuk lebih mudahnya, perhatikan tabel potensial elektroda standar berikut:
Perbedaan potensial dari kedua elektroda disebut sebagai beda potensial sel standar ( ). Rumusnya:
). Rumusnya:
Potensial sel dapat digunakan untuk memperkirakan spontan atau tidaknya suatu reaksi redoks. Reaksi redoks berlangsung spontan jika  (positif) dan tidak spontan jika
(positif) dan tidak spontan jika  (negatif).
(negatif).
2. Sel Elektrolisis
Apa yang dimaksud sel elektrolisis? Sel elektrolisis adalah sel eletrokimia yang mengubah energi listrik menjadi energi kimia. Pada sel elektrolisis katoda merupakan elektroda negatif, sedangkan anoda merupakan elektroda positif. Spesi yang mengalami reduksi adalah spesi (zat) yang mempunyai potensial elektroda lebih positif. Sedangkan spesi yang mengalami oksidasi adalah spesi (zat) yang mempunyai potensial elektroda lebih negatif. Dengan demikian, tidak selalu kation yang mengalami reduksi dan anion yang mengalami oksidasi. Dalam menuliskan reaksi sel elektrolisis kita harus memperhatikan beberapa hal berikut:
a. Reaksi Oksidasi
- Jika anoda terbuat dari Pt, Au, atau C, maka anoda tidak ikut teroksidasi. Contohnya: Ion
teroksidasi menjadi
dan gas
. Reaksinya:
- Jika anoda terbuat selain dari Pt, Au, atau C, maka anoda ikut teroksidasi. Contohnya: Anoda dari logam Ag maka reaksinya:
b. Reaksi Reduksi
- Ion
tereduksi menjadi gas
. Reaksinya:
- Ion-ion logam alkali dan alkali tanah serta
dan
tidak mengalami reduksi, yang tereduksi adalah pelarutnya. Reaksinya:
- Ion-ion logam selain alkali dan alkali tanah serta
dan
mengalami reduksi menjadi logamnya. reaksinya:
10 Contoh Soal Elektrolisis Kelas 12 beserta Jawabannya
Seperti yang telah kita pelajari, sel elektrolisis adalah sel yang mengubah energi listrik menjadi energi kimia. Arus listrik digunakan untuk melangsungkan reaksi redoks tak spontan. Supaya lebih paham mengenai sel elektrolisis, perhatikan 10 contoh soal elektrolisis berikut ini:
Soal No. 1
Pada elektrolisis Al2O3 (pengolahan Aluminium) sebanyak 102 kg dihasilkan Al …. (Al = 27, O =16)
A. 102 kg D. 30 kg
B. 80 kg E. 12 kg
C. 54 kg
Jawaban : C
Pembahasan:
Pembahasan:
Diketahui:
massa Al2O3 =102 kg = 102.000 gram; Mr Al2O3 = 102 gr/mol
massa Al2O3 =102 kg = 102.000 gram; Mr Al2O3 = 102 gr/mol
1 mol Al2O3 dihasilkan 2 mol Al3+
1000 mol Al2O3 dihasilkan 2000 mol Al3+
3e + Al3+ Al
Al
1 mol Al3+ ~ 1 mol Al1000 mol Al2O3 dihasilkan 2000 mol Al3+
3e + Al3+
2000 molAl3+ ~ 2000 mol Al
Jadi yang terjadi = 2000 mol
= 2000 x 27 gram
= 54.000 gram = 54 kg
Soal No. 2
 Cu
Cu
reaksi pada x adalah oksidasi pada anion.
 Ag = 0,80 +
Ag = 0,80 +
3,14 (paling besar)
 2OH– + H2
2OH– + H2
anoda : 2H2O 4H+ + O2 + 4e
4H+ + O2 + 4e
 Cl2 + 2e–
Cl2 + 2e–
Elektrolisis KNO3
Katoda : 2H2O 2OH– + H2(g)
2OH– + H2(g)
Anoda : 2H2O 4H+ + O2(g)
4H+ + O2(g)
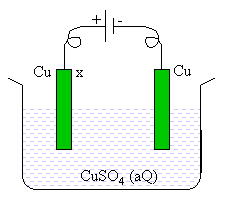
Pada elektrolisis seperti gambar di bawah ini persamaan yang menunjukkan reaksi pada elektroda X adalah ….
A. H2O(l)  2H+(aq) + ½O2 + 2e–
2H+(aq) + ½O2 + 2e–
B. Cu2+(aq) + 2e–  Cu(s)
Cu(s)
C. Cu(s)  Cu2+(aq) + 2e–
Cu2+(aq) + 2e–
D. 2H2O(l) + 2e–  H2(g) + 2OH–(aq)
H2(g) + 2OH–(aq)
E. 2H2O(l) + O2(l) + 4e–  4OH–(aq)
4OH–(aq)
Jawaban : C
Pembahasan :
Reaksi anoda = Cu Cu2+ + 2e
Cu2+ + 2e
Reaksi katoda = 2e + Cu2+ Pembahasan :
Reaksi anoda = Cu
reaksi pada x adalah oksidasi pada anion.
Soal No. 3
Data tabel E sel dalam volt. Pada tabel berikut harga E sel : Mg | Mg+2| | Pb+2 | Pb adalah ….
A. -2, 21 volt D. 2, 21 volt
B. -2, 47 volt E. 2, 68 volt
C. 2, 47 volt
Jawaban : C
Pembahasan:
Pembahasan:
Soal No. 4
Diketahui potensial elektroda :
Ag– (aq) + e  Ag(s) E0 = + 0,80 volt
Ag(s) E0 = + 0,80 volt
Ln3- (aq) + 3e  Ln(s) E0 = -0,34 volt
Ln(s) E0 = -0,34 volt
Mn2-(aq)+2e  Mg(s) E0 =-2,34 volt
Mg(s) E0 =-2,34 volt
Mn2-(aq) + 2e  Mn(s) E0 = -1,20 volt
Mn(s) E0 = -1,20 volt
Dua setengah sel di bawah ini yang potensialnya paling besar adalah ….
A. Mg | Mg2+ | | Ag+ | Ag D. Mn | Mn2+ | | Mg2+ | Mg
B. Ag | Ag+ | | Mg2+ | Mg E. Ag | Ag+ | | Ln2+ | Ln
C. Mn | Mn2+ | | Ln3+ | Ln
Jawaban : A
Pembahasan:
Pembahasan:
Mg  Mg2+ + 2e = 2,34
Mg2+ + 2e = 2,34
Ag+ + e 3,14 (paling besar)
Soal No. 5
Reaksi yang terjadi pada katode dari elektrolisis larutan Na2SO4 adalah ….
A. 2H2O(aq) + 2e  2OH–(aq) + H2(g)
2OH–(aq) + H2(g)
B. 2H+(aq) + 2e  H2(g)
H2(g)
C. Na+(aq) + e  Na(s)
Na(s)
D. SO42-(aq) + 2e  SO4(aq)
SO4(aq)
E. 4OH–(aq)  2H2O(aq) + O2(g) + 4e
2H2O(aq) + O2(g) + 4e
Jawaban : A
Pembahasan:
Na2SO4 2Na+ + SO42-
2Na+ + SO42-
katoda : 2H2O + 2e Pembahasan:
Na2SO4
anoda : 2H2O
Soal No. 6
Pada elektrolisis larutan garam logam alkali atau alkali tanah tidak dihasilkan logamnya karena ….
A. sifat oksidatornya lemah
B. sifat reduktornya lemah
C. garam halidanya mempunyai titik leleh tinggi
D. energi ionisasi tinggi dari logam lain
E. ion logamnya tidak mengalami reduksi
Jawaban : E
Pembahasan:
Pada elektrolisis larutan garam logam Alkali atau Alkali tanah tidak menghasilkan logam sebab :
– harga E° lebih kecil dari E° air
– ion logamnya tidak mengalami reduksi
Soal No. 7
Berapakah massa logam perak yang diendapkan jika arus listrik sebesar 5 Ampere dialirkan ke dalam larutan AgNO3 selama 2 jam …. (Ar : Ag = 108)
A. 24,90 gram D. 42,09 gram
B. 29,40 gram E. 49,20 gram
C. 40,29 gram
Jawaban : C
Soal No. 8
Pada saat sel aki bekerja, reaksi yang terjadi pada katode adalah ….
A. Pb(s) + SO42-(aq)  PbSO4(s) + 2e
PbSO4(s) + 2e
B. Pb2+(aq)+ 2e  Pb(s)
Pb(s)
C. PbO2(s) + 4H+(aq) + SO2-4(aq) + 2e  PbSO4(s) + H2O(l)
PbSO4(s) + H2O(l)
D. Pb2+(aq) + O2(g)  PbO2(s)
PbO2(s)
E. H2SO4(aq) 2H+(aq)+ SO2-4(aq)
2H+(aq)+ SO2-4(aq)
Jawaban : C
Pembahasan:
Reaksi : PbO2(s) + 4H+(aq)+ SO2-4(aq) + 2e  PbSO4(s) + H2O(l)
PbSO4(s) + H2O(l)
Soal No. 9
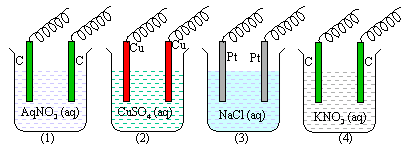
Perhatikan gambar elektrolisis berikut ini :
Elektrolisis yang menghasilkan gas H2 ditunjukkan pada gambar ….
A. 1 dan 2 D. 2 dan 4
B. 2 dan 3 E. 1 dan 4
C. 3 dan 4
Jawaban : C
Pembahasan:
Elektrolisis NaCl
Katoda : 2H2O + 2e– 2OH– + H2(g)
2OH– + H2(g)
Anoda : 2Cl– Pembahasan:
Elektrolisis NaCl
Katoda : 2H2O + 2e–
Elektrolisis KNO3
Katoda : 2H2O
Anoda : 2H2O
Soal No. 10
Pada reaksi elektrolisis larutan NiSO4 dengan elektroda Ag. Reaksi yang terjadi pada anoda adalah ….
A. Ni2+(aq) + 2e  Ni(s)
Ni(s)
B. Ag(aq)  Ag+(aq) + e
Ag+(aq) + e
C. Ni(s)  Ni2+(aq)+ 2e
Ni2+(aq)+ 2e
D. 2 H2O(l) + 2e  H2(g)+ 2 OH–(aq)
H2(g)+ 2 OH–(aq)
E. 2 H2O(l)  4 H+(aq) + O2(g) + 4e
4 H+(aq) + O2(g) + 4e
Jawaban : E
Pembahasan:
Reaksi Elektrolisis larutan NiSO4 dengan elektroda Ag
NiSO4(aq) Ni+2(aq) + SO-24(aq)
Ni+2(aq) + SO-24(aq)
NiSO4(aq)
Sisa asam dari (SO4-2 ; NO3– ; PO4-3) tidak dioksidasi yang mengalami oksidasi adalah pelarut air.
Anoda (oksidasi) : 2 H2O(aq)  4 H+(aq)+ O2(g) + 4e
4 H+(aq)+ O2(g) + 4e
Contoh Soal Hukum Faraday 2 dan Pembahasannya
Hukum Faraday II berbunyi “massa zat yang dihasilkan berbanding lurus dengan massa ekuivalennya untuk jumlah listrik yang sama.”
Soal No. 1
Pada elektrolisis larutan NiSO4 selama 45 menit menghasilkan endapan Ni sebanyak 9,75 gram. Berapa gram Ag yang dihasilkan jika arus dalam waktu yang sama dialirkan pada elektrolisis larutan AgNO3? (Ar Ni = 58,5; Ag = 108)
Pembahasan
Diketahui:
m Ni = 9,75 g
e Ni = 58,5/2 = 29,25
e Ag = 108/1 = 108
Ditanya: m Ag….?
Jawab:
m Ni : m Ag = e Ni : e Ag
9,75 : m Ag = 29,25 : 108
m Ag =  = 36 gr
= 36 gr
Jadi Ag yang dihasilkan jika arus dalam waktu yang sama dialirkan pada elektrolisis larutan AgNO3 sebesar 36 gr.
Soal No. 2
Jika arus listrik dialirkan melewati larutan
AgNO3 dan larutan CuSO4 yang disusun serim dan terendapkan 2,16 gram (Ar Ag = 108, Cu = 63,5). Hitunglah masa terendapkan!
Pembahasan
Diketahui:
m Ag = 2,16 g
e Ag = 108/1 = 108
e Cu = 63,5/2 = 31,75
Ditanya: m Cu….?
Jawab:
m Ag : m Cu = e Ag : e Cu
2,16 : m Cu = 108 : 31,75
m Cu= = 0,635 gr
= 0,635 gr
Jadi, massa tembaga yang diendapkan sebesar 0,635 gr.
Soal No. 3
Dalam elektrolisis larutan CuSO4 dengan elektroda inert dihasilkan 224 ml gas (STP) di anoda. Massa endapan yang didapat di katoda adalah … (Ar Cu = 63,5).
Pembahasan:
Diketahui:
(1) katoda : Cu2+ + 2e → Cu
(2) anoda : 2H2O → 4K+ + 4e + O2
(2) anoda : 2H2O → 4K+ + 4e + O2
m O2 = 224 ml = 0,224 l
e Cu = 63,5/1 = 63,5
e O2 = 22,4/2 = 11,2
Dit m Cu ….?
Jawab:
m Cu : m O2 = e Cu : e O2
m Cu : 0,224 = 63,5 : 11,2
m Cu= = 1,27 gr
= 1,27 gr
Jadi, massa endapan yang didapat di katoda sebesar 1,27 gr.
Soal No. 4
Ke dalam 2 sel larutan ZnSO4 dan larutan CuSO4 yang dihubungkan secara seri dialirkan arus listrik ternyata diendapkan 16,25 gram seng. Jika Ar Zn = 65 dan Ar Cu = 63,5 maka banyaknya tembaga yang mengendap adalah ….
Pembahasan
Diketahui:
m Zn = 16,25 gr
e Cu = 63,5/2 = 31,75
e Zn = 65/2 = 32,5
Ditanya: m Cu…?
Jawab:
m Cu : m Zn = e Cu : e Zn
m Cu : 16,25 = 31,75 : 32,5
m Cu =  = 15,875 gr
= 15,875 gr
Jadi, banyaknya tembaga yang mengendap sebesar 15,875 gr.










sangat bermanfaat bu, terimakasih
BalasHapusMaterinya oke
BalasHapusTrimakasih bu materinya
BalasHapusSangat bermanfaat ibu
BalasHapusTerimakasih Materinya bu sangat bermanfaat
BalasHapusTerimakasih atas materinya bu 🙏🏻🙏🏻
BalasHapusTerima kasih banyak BU materinya sangat bermanfaat🙏
BalasHapusTerimakasih bu sangat bermanfaat
BalasHapusTerimakasih ibu sangat bermanfaat
BalasHapus